Leksykon
Objaśnienie symboli stosowanych na opakowaniach firmy ZARYS International sp. z.o.o.
| Symbol | Nazwa symbolu | Objaśnienie symbolu | Odniesienie normatywne | Tytuł normy / aktu prawnego |
|---|---|---|---|---|

|
Oznakowanie zgodności CE | Oznakowanie, poprzez które wytwórca/producent wskazuje, że wyrób medyczny klasy I spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących zdrowia, bezpieczeństwa | MDR 2017/745 Artykuł 20, pkt.3. oraz Załącznik V | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Oznakowanie zgodności CE z numerem jednostki notyfikowanej | Oznakowanie, poprzez które wytwórca/producent wskazuje, że wyrób medyczny klasy I sterylnej lub IIa spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących zdrowia, bezpieczeństwa | Dyrektywa Rady 93/42/EWG Załącznik XII; MDR 2017/745 Artykuł 20, pkt.5. oraz Załącznik V | Dyrektywa Rady 93/42/EWG z dnia 14 czerwca 1993r. dotycząca wyrobów medycznych; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Oznakowanie, poprzez które producent wskazuje, że wyrób medyczny klasy I spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących zdrowia, bezpieczeństwa. Oznakowanie, poprzez które producent wskazuje, że środek ochrony indywidualnej kategorii III spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących ochrony zdrowia i bezpieczeństwa użytkowników. | Rozporządzenie PE i Rady (UE) 2017/745 Artykuł 20, pkt.6. oraz Załącznik V; Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 8, pkt.2.; Artykuł 17, pkt.3.; Załącznik II, pkt.1.4. (i) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016r. w sprawie środków ochrony indywidualnej | |

|
Wytwórca / Producent | Wskazuje wytwórcę wyrobu medycznego zgodnie z dyrektywą 93/42/EWG Wskazuje producenta wyrobu medycznego zgodnie z Rozporządzeniem PE i Rady (UE) 2017/745 Symbolowi temu towarzyszy nazwa i adres wytwórcy / producenta | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.1. (ISO 7000-3082); MDR 2017/745 Załącznik I, pkt.23.2. (c), pkt.23.3. (d) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Autoryzowany przedstawiciel we Wspólnocie Europejskiej | Wskazuje autoryzowanego przedstawiciele w WE Symbolowi temu towarzyszy nazwa i adres autoryzowanego przedstawiciela | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.2.; MDR 2017/745 Załącznik I, pkt.23.2. (d) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Data produkcji | Wskazuje datę wyprodukowania wyrobu medycznego Format daty: RRRR-MM-DD | Format daty: RRRR-MM-DD PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.3. (ISO 7000-2497); MDR 2017/745 Załącznik I, pkt.23.3. (h) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Użyć do daty | Wskazuje datę, po której wyrób medyczny nie powinien być używany Format daty: RRRR-MM-DD | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.4. (ISO 7000-2607); MDR 2017/745 Załącznik I, pkt.23.2. (i); pkt.23.3. (i) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Numer serii produkcyjnej | Wskazuje kod partii nadany przez wytwórcę, umożliwiający identyfikację partii lub serii Format kodu: XXRRMMXXXN/E/R/H | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.5. (ISO 7000-2492); MDR 2017/745 Załącznik I, pkt.23.2. (g) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Numer katalogowy | Wskazuje numer katalogowy nadany przez wytwórcę, umożliwiający identyfikację wyrobu medycznego Symbolowi temu towarzyszy numer nadany przez wytwórcę | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.6. (ISO 7000-2493); MDR 2017/745 Załącznik I, pkt.23.2. (b | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Importer | Wskazuje podmiot importujący wyrób medyczny do lokalnego użycia Symbolowi temu towarzyszy nazwa i adres importera | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.8. (ISO 7000-3725); MDR 2017/745 Artykuł 13, pkt.3. | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Dystrybutor | Wskazuje podmiot dystrybuujący wyrób medyczny do lokalnego użycia; Symbolowi temu towarzyszy nazwa i adres dystrybutora; | EN ISO 15223-1:2021 Nr ref. symbolu 5.1.9. (ISO 7000-3724) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Kraj produkcji | Wskazuje kraj produkcji wyrobu „CC” powinno zostać zastąpione dwuliterowym symbolem kraju zgodnie z ISO 3166-1 Obok tego symbolu można dodać datę produkcji | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.1.11. (ISO 7000-6049) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Wysterylizowany tlenkiem etylenu | Wskazuje wyrób medyczny, który został wysterylizowany przy użyciu tlenku etylenu | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.3. (ISO 7000-2501); MDR 2017/745 Załącznik I, pkt.23.2. (l), pkt.23.3. (b),(c) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Wysterylizowany radiacyjnie | Wskazuje wyrób medyczny, który został wysterylizowany za pomocą promieniowania | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.4. (ISO 7000-2502); MDR 2017/745 Załącznik I, pkt.23.2. (l), pkt.23.3. (b),(c) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Wysterylizowany parą wodną lub suchym ciepłem | Wskazuje wyrób medyczny, który został wysterylizowany parą wodną lub suchym ciepłem | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.5. (ISO 7000-2503); MDR 2017/745 Załącznik I, pkt.23.2. (l), pkt.23.3. (b),(c) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie resterylizować | Wskazuje wyrób medyczny, który nie może być sterylizowany ponownie Tego symbolu należy używać tylko wtedy, gdy towarzyszy mu symbol „STERILE” (5.2.3./5.2.4./5.2.5.) | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.6. (ISO 7000-2608); MDR 2017/745 Załącznik I, pkt.23.2. (m), pkt.23.3. (j) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Niesterylny | Wskazuje wyrób medyczny, który nie był poddawany procesowi sterylizacji | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.7. (ISO 7000-2609); MDR 2017/745 Załącznik I, pkt.23.2. (m) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie używać, jeżeli opakowanie zostało uszkodzone | Wskazuje wyrób medyczny, który nie powinien być używany, jeśli opakowanie zostało uszkodzone lub otwarte | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.8. (ISO 7000-2606); MDR 2017/745 Załącznik I, pkt.23.2. (m), pkt.23.3. (j) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Pojedynczy system bariery sterylnej | Wskazuje użytkownikowi warstwę opakowania, która tworzy system bariery sterylnej, aby wykonać odpowiednią aseptyczną prezentację zawartości, minimalizując ryzyko dla pacjenta | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.11. (ISO 7000-3707); MDR 2017/745 Załącznik I, pkt.23.3. (a) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Pojedynczy system bariery sterylnej z opakowaniem ochronnym wewnątrz | Wskazuje, że istnieje jeden sterylny system barierowy z opakowaniem ochronnym w środku. Opakowanie ochronne umieszczone wewnątrz systemu bariery sterylnej ma na celu zapobieganie uszkodzeniom zawartości lub pomoc w aseptycznej prezentacji. Nie stanowi bariery mikrobiologicznej w celu utrzymania sterylności | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.13. (ISO 7000-3708); MDR 2017/745 Załącznik I, pkt.23.3. (a) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Pojedynczy system bariery sterylnej z opakowaniem ochronnym na zewnątrz | Wskazuje, że istnieje jeden sterylny system barierowy z opakowaniem ochronnym na zewnątrz. Opakowanie ochronne umieszczone na zewnątrz systemu bariery sterylnej jest zaprojektowane tak, aby zapobiec uszkodzeniu systemu bariery sterylnej i jego zawartości lub aby pomóc w aseptycznej prezentacji. Nie stanowi ono bariery dla mikroorganizmów w celu utrzymania sterylności. | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.13. (ISO 7000-3709); MDR 2017/745 Załącznik I, pkt.23.3. (a) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Podwójny system bariery sterylnej | Wskazuje użytkownikowi, że istnieje podwójny system bariery sterylnej, aby wykonać odpowiednią aseptyczną prezentację zawartości, minimalizując ryzyko dla pacjenta. | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.2.14. (ISO 7000-3704); MDR 2017/745 Załącznik I, pkt.23.3. (a) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Kruchy, obchodzić ostrożnie | Wskazuje wyrób medyczny, który może zostać zepsuty lub uszkodzony, jeżeli nie będzie się z nim ostrożnie obchodzić. | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.3.1. (ISO 7000-0621); MDR 2017/745 Załącznik I, pkt.23.2. (k) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Trzymać z dala od światła słonecznego | Wskazuje wyrób medyczny, który wymaga ochrony przed źródłami światła | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.3.2. (ISO 7000-0624); MDR 2017/745 Załącznik I, pkt.23.2. (k) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Chronić przed wilgocią | Wskazuje wyrób medyczny, który wymaga ochrony przed wilgocią | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.3.4. (ISO 7000-0626); MDR 2017/745 Załącznik I, pkt.23.2. (k) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Dopuszczalna temperatura | Wskazuje zakres temperatur, na które wyrób medyczny może być bezpiecznie narażony Górną i dolną granicę zakresu dopuszczalnej temperatury należy skazać w sąsiedztwie górnej i dolnej poziomej linii, odpowiednio | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.3.7. (ISO 7000-0632); MDR 2017/745 Załącznik I, pkt.23.2. (k) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Ograniczenie wilgotności | Wskazuje zakres wilgotności, na którą wyrób medyczny może być bezpiecznie narażony Ograniczenia wilgotności należy skazać w sąsiedztwie górnej i dolnej poziomej linii, odpowiednio | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.3.8. (ISO 7000-2620); MDR 2017/745 Załącznik I, pkt.23.2. (k) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie używać powtórnie | Wskazuje wyrób medyczny, który jest przeznaczony tylko do jednorazowego użycia lub do użycia u jednego pacjenta podczas jednego zabiegu | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.2. (ISO 7000-1051); MDR 2017/745 Załącznik I, pkt.23.2. (n) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Wielokrotne użycie przez jednego pacjenta | Wskazuje wyrób medyczny, który może być używany wielokrotnie (wiele procedur) u jednego pacjenta; | EN ISO 15223-1:2021 Nr ref. symbolu 5.4.12. (ISO 7000-3706) MDR 2017/745 Załącznik I, pkt.4. (c) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Zajrzyj do instrukcji używania | Wskazuje, że użytkownik powinien zapoznać się z instrukcja używania | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.3. (ISO 7000-1641); MDR 2017/745 Załącznik I, pkt.23.2. (k), pkt.23.3. (j) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Zajrzyj do elektronicznej instrukcji używania | Wskazuje, że użytkownik powinien zapoznać się z elektroniczną instrukcja używania oraz gdzie można znaleźć elektroniczną instrukcję obsługi (eIFU) oraz leksykon symboli | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.3. (ISO 7000-1641); MDR 2017/745 Załącznik I, pkt.23.2. (k), pkt.23.3. (j) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Ostrzeżenie | Wskazuje, że należy zachować ostrożność podczas obsługi urządzenia lub sterowania w pobliżu miejsca, w którym znajduje się symbol, lub aby wskazać, że obecna sytuacja wymaga świadomości operatora lub działania operatora w celu uniknięcia niepożądanych konsekwencji. | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.4. (ISO 7000-0434A); MDR 2017/745 Załącznik I, pkt.23.2. (m) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Zawiera lub obecny jest lateks kauczuku naturalnego | Wskazuje obecność kauczuku naturalnego lub wysuszonego kauczuku naturalnego, jako materiału konstrukcyjnego w wyrobie medycznym lub opakowaniu wyrobu medycznego | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.5. (ISO 7000-2725); MDR 2017/745 Załącznik I, pkt.23.2. (m) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
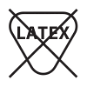
Nie zawiera lateksu kauczuku naturalnego | Wskazuje brak kauczuku naturalnego lub wysuszonego kauczuku naturalnego, jako materiału konstrukcyjnego w wyrobie medycznym | PN-EN ISO 15223-1:2022-01 Załącznik B Stosowanie symbolu negacji | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Zawiera niebezpieczne substancje | Wskazuje, że wyrób medyczny zawiera substancje, które mogą być rakotwórcze, mutagenne, działające szkodliwie na rozrodczość (CMR) lub substancje zaburzające funkcjonowanie układu hormonalnego | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.4.10. (ISO 7000-3723); MDR 2017/745 Załącznik I, pkt.10.4.5., pkt.23.2. (f) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Zawiera lub obecny jest ftalan 2-etyloheksylu (DEHP) | Wskazuje wyrób medyczny pochodzący z lub wyprodukowany z surowców zawierających ftalan: ftalan 2-etyloheksylu (DEHP) | PN-EN 15986:2011 Załącznik A Rys. A.1; MDR 2017/745 Załącznik I, pkt.10.4.5., pkt.23.2. (f) | Symbole używane w oznakowaniu wyrobów medycznych – Wymagania dotyczące oznakowania wyrobów medycznych zawierających ftalany; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
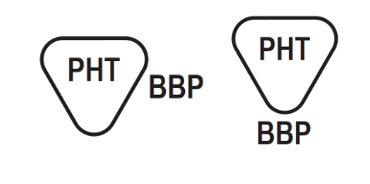
Zawiera lub obecny jest ftalan benzylu-butylu (BBP) | Wskazuje wyrób medyczny pochodzący z lub wyprodukowany z surowców zawierających ftalan: ftalan benzylu-butylu (BBP) | PN-EN 15986:2011 Załącznik A Rys. A.5; MDR 2017/745 Załącznik I, pkt.10.4.5., pkt.23.2. (f) | Symbole używane w oznakowaniu wyrobów medycznych – Wymagania dotyczące oznakowania wyrobów medycznych zawierających ftalany; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
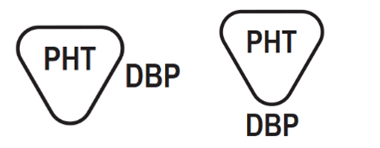
Zawiera lub obecny jest ftalan dibutylu (DBP) | Wskazuje wyrób medyczny pochodzący z lub wyprodukowany z surowców zawierających ftalan: ftalan dibutylu (DBP) | PN-EN 15986:2011 Załącznik A Rys. A.3; MDR 2017/745 Załącznik I, pkt.10.4.5., pkt.23.2. (f) | Symbole używane w oznakowaniu wyrobów medycznych – Wymagania dotyczące oznakowania wyrobów medycznych zawierających ftalany; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
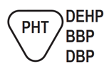
Zawiera lub obecne są ftalany DEHP, BBP oraz DBP | Wskazuje wyrób medyczny pochodzący z lub wyprodukowany z surowców zawierających ftalany: ftalany DEHP, BBP oraz DBP | PN-EN 15986:2011 Załącznik A Rys. A.7; MDR 2017/745 Załącznik I, pkt.10.4.5., pkt.23.2. (f) | Symbole używane w oznakowaniu wyrobów medycznych – Wymagania dotyczące oznakowania wyrobów medycznych zawierających ftalany; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
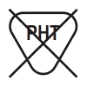
Nie zawiera ftalanów | Wskazuje, że wyrób medyczny nie zawiera ftalanów | PN-EN 15986:2011 Załącznik B Stosowanie symbolu negacji | Symbole używane w oznakowaniu wyrobów medycznych – Wymagania dotyczące oznakowania wyrobów medycznych zawierających ftalany |

|
Apirogenny | Wskazuje wyrób medyczny, który jest apirogenny | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.6.3. (ISO 7000-2724) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Krople na mililitr | Wskazuje liczbę kropli na mililitr Liczbę 20 pokazano jako przykład i należy zastąpić ją przez odpowiednią liczbę kropli na mililitr | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.6.4. (ISO 7000-2726); MDR 2017/745 Załącznik I, pkt.23.2. (b) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Filtr płynu o wielkości porów | Wskazuje infuzyjny lub transfuzyjny system wyrobu medycznego zawierający filtr o określonej nominalnej wielkości porów Liczbę 15 pokazano jako przykład i należy zastąpić ją odpowiednią wielkością porów | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.6.5. (ISO 7000-2727); MDR 2017/745 Załącznik I, pkt.23.2. (b) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Przyrząd do podawania grawitacyjnego | Wskazuje przyrząd do prowadzenia wlewów kroplowych lub przyrząd do podawania krwi i preparatów krwiopochodnych metodą grawitacyjną; | ||

|
Zawór jednokierunkowy | Wskazuje wyrób medyczny z zaworem, który umożliwia przepływ tylko w jednym kierunku | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.6.6. (ISO 7000-2728); MDR 2017/745 Załącznik I, pkt.23.2. (b) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Kąt płaski | Wskazuje miarę kąta płaskiego; Miarę kąta należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie); | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Rozmiar | Wskazuje rozmiar wyrobu; Rozmiar należy wskazać w sąsiedztwie symbolu (po prawej stronie); | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Wyrób medyczny | Wskazuje, że produkt jest wyrobem medycznym | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.7.7.; MDR 2017/745 Załącznik I, pkt.23.2. (q) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Niepowtarzalny kod identyfikacyjny wyrobu (UDI) | Wskazuje kod kreskowy zawierający kod UDI; Powinien być użyty, gdy na etykiecie znajduje się wiele nośników danych (kodów kreskowych), np. na kartonie transportowym; Jeżeli jest używany, symbol ten powinien znajdować się w sąsiedztwie nośnika niepowtarzalnego kodu identyfikacyjnego wyrobu; | EN ISO 15223-1:2021 Nr ref. symbolu 5.7.10. MDR 2017/745 Załącznik I, pkt.23.2. (h) | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
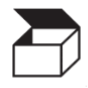
Jednostka opakowania | Wskazuje liczbę sztuk w opakowaniu Liczbę sztuk należy skazać w pustym polu na froncie Format: 1 dla jednostki 50 x 1 dla opakowania zbiorczego 50 sztuk pakowanych indywidualnie 50 dla opakowania zbiorczego 50 sztuk NIE pakowanych indywidualnie 20 x 50 dla opakowania zbiorczego zawierającego 20 opakowań po 50 sztuk | ISO 7000 Nr ref. symbolu 2794;; MDR 2017/745 Załącznik I, pkt.23.2. (b) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Jednostka opakowania | Wskazuje liczbę sztuk w opakowaniu jednostkowym; | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Średnica zewnętrzna | Wskazuje odniesienie do średnicy zewnętrznej Średnicę zewnętrzną należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie) | ISO 7000 Nr ref. symbolu 5846; MDR 2017/745 Załącznik I, pkt.23.2. (b) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Średnica zewnętrzna | Wskazuje odniesienie do średnicy zewnętrznej Średnicę zewnętrzną należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie) | ISO 7000 Nr ref. symbolu 5846; MDR 2017/745 Załącznik I, pkt.23.2. (b) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
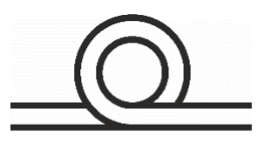
Długość | Wskazuje długość drenu Długość należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie) | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
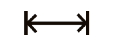
|
Długość | Wskazuje długość rurki Długość należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie) | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Rozmiar mankietu | Wskazuje rozmiar mankietu Rozmiar mankietu należy wskazać w sąsiedztwie symbolu wraz z jednostką miary (po prawej stronie) | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Waga pacjenta | Wskazuje wagę pacjenta, dla którego dedykowany jest dany rozmiar maski krtaniowej; Liczbę „X” należy zastąpić wagą pacjenta; | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
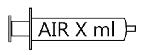
|
Maksymalna objętość powietrza, którym należy napompować mankiet | Wskazuje maksymalną objętość powietrza, którym należy napompować mankiet maski krtaniowej; Liczbę „X” należy zastąpić objętością powietrza; | MDR 2017/745 Załącznik I, pkt.23.2. (b | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Bezpieczny dla rezonansu magnetycznego | Służy do identyfikacji wyrobów, które nie stwarzają znanych zagrożeń w środowisku rezonansu magnetycznego | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Kolor | Wskazuje na kolor wyrobu Kolor zielony pokazano jako przykład i należy zastąpić go przed kółko w odpowiednim kolorze; w przypadku koloru białego – białe kółko z obramowaniem w wiodącym kolorze opakowania | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Rozmiar | Wskazuje rozmiar wyrobu Litera „L” pokazano jako przykład i należy zastąpić ją przez odpowiedni rozmiar | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Gramatura | Wskazuje gramaturę materiału, z którego wykonany jest wyrób Liczbę 25 pokazano jako przykład i należy zastąpić ją przez odpowiednią gramaturę | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Typ włókniny | Wskazuje typ włókniny, z której wykonany jest wyrób Litery „PF” pokazano jako przykład i należy zastąpić je przez odpowiedni typ włókniny | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Liczba nitek w gazie | Wskazuje liczbę nitek w gazie na cm2 Liczbę 17 pokazano jako przykład i należy zastąpić ją przez odpowiednią liczbę nitek | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Liczba warstw | Wskazuje liczbę warstw w wyrobie Liczbę 16 pokazano jako przykład i należy zastąpić ją przez odpowiednią liczbę warstw | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Miejsce otwierania opakowania | Wskazuje użytkownikowi miejsce otwierania opakowania, które tworzy system bariery sterylnej, aby wykonać odpowiednią aseptyczną prezentację zawartości, minimalizując ryzyko dla pacjenta Symbol ten stosowany jest w przypadku opakowania, które należy otworzyć poprzez oddzielenie od siebie jego górnej i dolnej warstwy; strzałka wskazuje kierunek rozdzielenia warstw | MDR 2017/745 Załącznik I, pkt.23.2. (k) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Miejsce otwierania opakowania | Wskazuje użytkownikowi miejsce otwierania opakowania, które tworzy system bariery sterylnej, aby wykonać odpowiednią aseptyczną prezentację zawartości, minimalizując ryzyko dla pacjenta Symbol ten stosowany jest w przypadku opakowania, które należy rozedrzeć we wskazanym przez symbol miejscu | MDR 2017/745 Załącznik I, pkt.23.2. (k) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Prać ręcznie | Wskazuje, że czyszczenie artykułu włókienniczego jest dozwolone tylko przez pranie ręczne | EN ISO 3758:2023 (ISO 7000-3125) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Pranie, normalny proces, maksymalnie 40 stopni Celsjusza | Wskazuje, że czyszczenie artykułu włókienniczego jest dozwolone przy użyciu normalnego procesu prania w maksymalnej temperaturze 40 stopni Celsjusza. | EN ISO 3758:2023 (ISO 7000-3089) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Pranie, normalny proces, maksymalnie 95 stopni Celsjusza | Wskazuje, że czyszczenie artykułu włókienniczego jest dozwolone przy użyciu normalnego procesu prania w maksymalnej temperaturze 95 stopni Celsjusza; | EN ISO 3758:2023 (ISO 7000-3097) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Nie używać wybielacza | Wskazuje wyrób, do którego nie należy używać wybielacza | EN ISO 3758:2023 (ISO 7000-3124) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Nie suszyć mechanicznie | Wskazuje wyrób, którego nie powinno się suszyć w suszarce bębnowej | EN ISO 3758:2023 (ISO 7000-3109) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie prasować | Wskazuje wyrób, którego nie należy prasować | EN ISO 3758:2023 (ISO 7000-3113) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie czyścić chemicznie | Wskazuje wyrób, którego nie należy czyścić chemicznie | EN ISO 3758:2023 (ISO 7000-3114) MDR 2017/745 Załącznik I, pkt.23.2. (k) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
Liczba par | Wskazuje liczbę par wyrobu w opakowaniu; | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
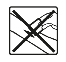
Nie stosować bezpośrednio na rany | Wskazuje wyrób, którego nie należy stosować bezpośrednio na rany lub uszkodzony naskórek | MDR 2017/745 Załącznik I, pkt.23.2. (k) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |
|
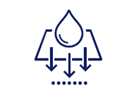
Zawiera superabsorbent | Wskazuje wyrób, który posiada wkład chłonny z superabsorbentem; | - | - |

|
Wyrób medyczny do diagnostyki in vitro | Wskazuje wyrób medyczny, który jest przeznaczony do zastosowania jako wyrób medyczny do diagnostyki in vitro | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.5.2. | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Zawartość wystarczająca do testów | Wskazuje łączną liczbę testów IVD, które można wykonać za pomocą IVD. | PN-EN ISO 15223-1:2022-01 Nr ref. symbolu 5.5.5. | Wyroby medyczne -- Symbole do stosowania wraz z informacjami dostarczanymi przez producenta -- Część 1: Wymagania ogólne |

|
Dopuszczalny poziom jakości EN455-1, EN 374-2 | Wskazuje granicę akceptowanej jakości; | EN 455-1:2020+A1:2022 EN ISO 374-2:2019 | Rękawice medyczne do jednorazowego użytku -- Część 1: Wymagania i badania na nieobecność dziur. Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 2: Wyznaczanie odporności na przesiąkanie |

|
Rękawice bezpudrowe | Oznakowanie, za pomocą którego producent wskazuje, że wyrób medyczny nie zawiera środków pudrujacych, występuje w wersji bezpudrowej | - | - |

|
Liczba rękawic | Wskazuje liczbę sztuk rękawic w opakowaniu; | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Liczba par rękawic | Wskazuje liczbę par rękawic w opakowaniu; | MDR 2017/745 Załącznik I, pkt.23.2. (b) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Zawiera lub obecny jest alergen typu IV | Wskazuje, że wyrób medyczny zawiera potencjalne alergeny chemiczne typu IV; | EN 455-3:2023 (ISO 7000-2725) MDR 2017/745 Załącznik I, pkt.23.2. (m) | Rękawice medyczne do jednorazowego użytku Część 3: Wymagania i badania w ocenie biologicznej; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Limit układania w stos | Wskazuje, że opakowania transportowe nie mogą być układane w pionie poza określoną liczbę, ani ze względu na rodzaj opakowania transportowego, ani z powodu charakteru samych przedmiotów. Liczbę „n” należy zastąpić maksymalną liczbą dozwolonych opakowań Liczba „n” nie obejmuje dolnego opakowania w stosie | ISO 7000 Nr ref. symbolu 2403; MDR 2017/745 Załącznik I, pkt.23.2. (k) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Tą stroną w górę | Wskazuje prawidłową pozycję pionową opakowania transportowego | ISO 7000 Nr ref. symbolu 0623; MDR 2017/745 Załącznik I, pkt.23.2. (k) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017r. w sprawie wyrobów medycznych |

|
Nie używać haków | Wskazuje, że haki nie mogą być używane do przenoszenia opakowania transportowego | ISO 7000 Nr ref. symbolu 0622 | Symbole graficzne stosowane na urządzeniach; |
|
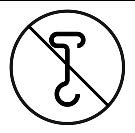
Nie używać haków | Wskazuje, że haki nie mogą być używane do przenoszenia opakowania transportowego | ||

|
Nie używać ostrych narzędzi | Wskazuje, że ostre narzędzia nie mogą być używane do otwierania opakowania transportowego | ||

|
Nie deptać | Wskazuje, że nie można stawać na opakowaniu transportowym | ||

|
Nadający się do przetworzenia | Wskazanie, że oznaczone opakowanie transportowe jest częścią procesu odzysku lub recyklingu | ISO 7000 Nr ref. symbolu 1135 | Symbole graficzne stosowane na urządzeniach; |

|
Polietylen małej gęstości | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 1 Nr symbolu 4 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Polietylen dużej gęstości | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 1 Nr symbolu 2 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Polipropylen | Wskazuje materiał, z którego wykonane jest opakowanie; | Załącznik nr 1 Nr symbolu 2 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Tektura falista | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 2 Nr symbolu 1 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Tektura płaska | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 2 Nr symbolu 2 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Papier | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 2 Nr symbolu 3 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Papier i tektura/plastik/ aluminium | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 7 Nr symbolu 5 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Inne tworzywa sztuczne | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 1 Nr symbolu 7 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Mieszane | Wskazuje, że opakowanie wykonane jest z różnych/mieszanych materiałów | Załącznik nr 2 Nr symbolu 1 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Znak zgodności z wymaganiami rynku ukraińskiego | Oznakowanie, poprzez które producent wskazuje, że wyrób medyczny klasy I spełnia obowiązujące wymagania odpowiednich ukraińskich przepisów dotyczących zdrowia i bezpieczeństwa; | ||

|
Znak zgodności z wymaganiami rynku ukraińskiego z numerem jednostki oceniającej zgodność | Oznakowanie, poprzez które wytwórca / producent wskazuje, że wyrób medyczny klasy I sterylnej IIa lub IIb spełnia obowiązujące wymagania odpowiednich ukraińskich przepisów dotyczących zdrowia i bezpieczeństwa; | ||

|
Znak zgodności z wymaganiami rynku brytyjskiego | Oznakowanie, poprzez które producent wskazuje, że wyrób medyczny klasy I spełnia obowiązujące wymagania odpowiednich przepisów dotyczących zdrowia i bezpieczeństwa w Wielkiej Brytanii; | ||

|
Certyfikacja zgodności z normą ISO 14001 | Oznakowanie, za pomocą którego producent wskazuje, że produkcja wyrobu medycznego spełnia wymagania normy ISO 14001, która dotyczy systemu zarządzania środowiskowego; | - | - |

|
Certyfikacja zgodności z normą ISO 13485 | Oznakowanie, za pomocą którego producent wskazuje, że produkcja wyrobu medycznego spełnia wymagania normy ISO 13485, która dotyczy systemu zarządzania jakością dla producentów wyrobów medycznych; | - | - |

|
Upoważniony przedstawiciel na rynek szwajcarski | Wskazuje upoważnionego przedstawiciela na rynek szwajcarski; Symbolowi temu towarzyszy nazwa i adres upoważnionego przedstawiciela; | - | - |
| Symbol | Nazwa symbolu | Objaśnienie symbolu | Odniesienie normatywne | Tytuł normy / aktu prawnego |
|---|---|---|---|---|

|
Oznakowanie zgodności CE | Oznakowanie, poprzez które producent wskazuje, że środek ochrony indywidualnej kategorii I spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących ochrony zdrowia i bezpieczeństwa użytkowników | Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 8, pkt.2. Artykuł 16 i 17 | Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Oznakowanie zgodności CE z numerem jednostki notyfikowanej | Oznakowanie, poprzez które producent wskazuje, że środek ochrony indywidualnej kategorii III spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących ochrony zdrowia i bezpieczeństwa użytkowników | Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 8, pkt.2. Artykuł 17, pkt.3. | Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Oznakowanie, poprzez które producent wskazuje, że wyrób medyczny klasy I spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących zdrowia, bezpieczeństwa Oznakowanie, poprzez które producent wskazuje, że środek ochrony indywidualnej kategorii III spełnia obowiązujące wymagania odpowiednich europejskich przepisów dotyczących ochrony zdrowia i bezpieczeństwa użytkowników | Rozporządzenie PE i Rady (UE) 2017/745 Artykuł 20, pkt.6 oraz Załącznik V; Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 8, pkt.2.; Artykuł 17, pkt.3.; Załącznik II, pkt.1.4. (i) | Rozporządzenie PE i Rady (UE) 2017/745 z dnia 5 kwietnia 2017 r. w sprawie wyrobów medycznych; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej | |

|
Producent | Wskazuje producenta ŚOI zgodnie z Rozporządzeniem PE i Rady (UE) 2016/425 Symbolowi temu towarzyszy nazwa i adres wytwórcy / producenta | ISO 7000 Nr ref. symbolu 3082; Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 8, pkt.6. | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Autoryzowany przedstawiciel we Wspólnocie Europejskiej | Wskazuje autoryzowanego przedstawiciele w WE Symbolowi temu towarzyszy nazwa i adres autoryzowanego przedstawiciela | Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 9 | Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Importer | Wskazuje podmiot importujący ŚOI do lokalnego użycia Symbolowi temu towarzyszy nazwa i adres importera | ISO 7000 Nr ref. symbolu 3725; Rozporządzenie PE i Rady (UE) 2016/425 Artykuł 10, pkt.3. | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
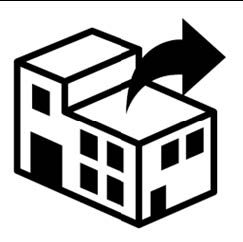
Dystrybutor | Wskazuje podmiot dystrybuujący ŚOI do lokalnego użycia; Symbolowi temu towarzyszy nazwa i adres dystrybutora; | ISO 7000 Nr ref. symbolu 3724 | Symbole graficzne stosowane na urządzeniach; |

|
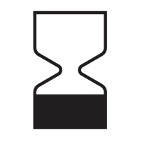
Data produkcji | Wskazuje datę wyprodukowania ŚOI Format daty: RRRR-MM-DD | ISO 7000 Nr ref. symbolu 2497) | Symbole graficzne stosowane na urządzeniach |
|
Użyć do daty | Wskazuje datę, po której ŚOI nie powinien być używany Format daty: RRRR-MM-DD | ISO 7000 Nr ref. symbolu 2607; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (e) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Kod partii | Wskazuje kod partii nadany przez producenta, umożliwiający identyfikację partii lub serii Format kodu: XXRRMMXXXN/E/R/H | ISO 7000 Nr ref. symbolu 2492 | Symbole graficzne stosowane na urządzeniach |

|
Numer katalogowy | Wskazuje numer katalogowy nadany przez producenta, umożliwiający identyfikację ŚOI | ISO 7000 Nr ref. symbolu 2493 | Symbole graficzne stosowane na urządzeniach |
|
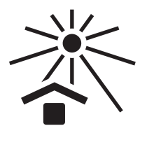
Trzymać z dala od światła słonecznego | Wskazuje ŚOI, który wymaga ochrony przed źródłami światła | ISO 7000 Nr ref. symbolu 0624; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Chronić przed wilgocią | Wskazuje ŚOI, który wymaga ochrony przed wilgocią | ISO 7000 Nr ref. symbolu 0626; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
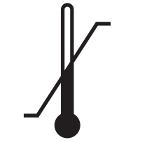
Dopuszczalna temperatura | Wskazuje zakres temperatur, na które ŚOI może być bezpiecznie narażony Górną i dolną granicę zakresu dopuszczalnej temperatury należy skazać w sąsiedztwie górnej i dolnej poziomej linii, odpowiednio | ISO 7000 Nr ref. symbolu 0632; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Ograniczenie wilgotności | Wskazuje zakres wilgotności, na którą ŚOI może być bezpiecznie narażony Ograniczenia wilgotności należy skazać w sąsiedztwie górnej i dolnej poziomej linii, odpowiednio | ISO 7000 Nr ref. symbolu 2620; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
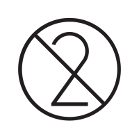
Nie używać powtórnie | Wskazuje ŚOI, który jest przeznaczony tylko do jednorazowego użycia | ISO 7000 Nr ref. symbolu 1051 | Symbole graficzne stosowane na urządzeniach |

|
Zawiera lub obecny jest lateks kauczuku naturalnego | Wskazuje obecność kauczuku naturalnego lub wysuszonego kauczuku naturalnego, jako materiału konstrukcyjnego w ŚOI lub opakowaniu ŚOI | ISO 7000 Nr ref. symbolu 2725 | Symbole graficzne stosowane na urządzeniach |

|
Nie zawiera lateksu kauczuku naturalnego | Wskazuje brak kauczuku naturalnego lub wysuszonego kauczuku naturalnego, jako materiału konstrukcyjnego w wyrobie medycznym | ||

|
Zajrzyj do instrukcji używania | Wskazuje, że użytkownik powinien zapoznać się z instrukcja używania | ISO 7000 Nr ref. symbolu 1641; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Rozmiar | Wskazuje rozmiar produktu Litera „L” pokazano jako przykład i należy zastąpić ją przez odpowiedni rozmiar | ||
|
Ochrona przed chemikaliami | Wskazuje, że odzież lub materiał zapewnia ochronę przed chemikaliami | ISO 7000 Nr ref. symbolu 2414 | Symbole graficzne stosowane na urządzeniach |
|
Ochrona przed natryskiem ciekłych substancji chemicznych, typ 4 | Wskazuje odzież ochronną typu 4, która jest przeznaczona do stosowania w przypadku zagrożeń związanych z nieprzepuszczalnością wobec substancji chemicznych podczas czynności, dla których wymagana jest bariera dla przenikania cieczy Litera „B” wskazuje, że odzież lub materiał zapewnia ochronę przed zagrożeniami biologicznymi (mikroorganizmami) zgodnie z EN 14126:2003 | EN 14605:2005+A1:2009 | Odzież chroniąca przed ciekłymi chemikaliami -- Wymagania dotyczące odzieży ochraniającej całe ciało, z połączeniami nieprzepuszczającymi cieczy w postaci płynnej (Typ 3) lub rozpylonej (Typ 4), łącznie z wyrobami zapewniającymi tylko częściową ochronę ciała (Typy PB[3] i PB[4]) |
|
Ochrona przed obecnymi w powietrzu cząstkami stałymi, typ 5 | Wskazuje odzież ochronną typu 5, która jest przeznaczona do stosowania w przypadku ryzyka narażenia na działanie produktów chemicznych z odpornością na przenikanie cząstek stałych rozproszonych w powietrzu Litera „B” wskazuje, że odzież lub materiał zapewnia ochronę przed zagrożeniami biologicznymi (mikroorganizmami) zgodnie z EN 14126:2003 | EN ISO 13982-1:2004 | Odzież chroniąca przed cząstkami stałymi -- Część 1: Wymagania dotyczące odzieży chroniącej całe ciało przed działaniem stałych cząstek substancji chemicznych unoszących się w powietrzu (typ 5 odzieży) |

|
Ochrona przed ograniczonym natryskiem ciekłych substancji chemicznych, typ 6 | Wskazuje odzież ochronną typu 6, która jest przeznaczona do stosowania w przypadku narażenia na lekki rozprysk, aerozole w płynie lub rozpryski pod niskim ciśnieniem, o małej objętości, wobec których nie jest wymagana pełna bariera dla przenikania cieczy, czyli gdy użytkownik jest w stanie podjąć w odpowiednim czasie właściwe działanie, kiedy jego odzież zostaje zanieczyszczona Litera „B” wskazuje, że odzież lub materiał zapewnia ochronę przed zagrożeniami biologicznymi (mikroorganizmami) zgodnie z EN 14126:2003 | EN 13034:2005+A1:2009 | Odzież chroniąca przed ciekłymi chemikaliami -- Wymagania dotyczące odzieży zapewniającej ograniczoną skuteczność ochrony przed ciekłymi chemikaliami (Typ 6 i Typ PB[6] odzieży) |

|
Ochrona przed elektrycznością statyczną | Wskazuje, że odzież lub materiał zapewnia ochronę przed elektrycznością statyczną. | EN 1149-5:2008 (ISO 7000-2415) | Odzież ochronna -- Właściwości elektrostatyczne -- Część 5: Wymagania materiałowe i konstrukcyjne |

|
Ochrona przed narażeniem na czynniki zakaźne, typ 4B, 5B, 6B | Wskazuje, że odzież lub materiał zapewnia ochronę przed zagrożeniami biologicznymi (mikroorganizmami) | EN 14126:2003 (ISO 7000-2491) | Odzież ochronna -- Wymagania i metody badań dla odzieży chroniącej przed czynnikami infekcyjnymi |

|
Ochrona przed skażonymi radioaktywnie cząsteczkami | Wskazuje, że odzież lub materiał zapewnia ochronę przed skażeniem cząstkami radioaktywnymi. | EN 1073-2:2002 (ISO 7000-2484) | Odzież chroniąca przed skażeniami promieniotwórczymi -- Część 2: Wymagania i metody badań dotyczące niewentylowanej odzieży chroniącej przed skażeniami cząstkami promieniotwórczymi |

|
Koniec okresu przechowywania | Wskazuje datę, po której ŚOI nie powinien być używany Format daty: RRRR/MM Datę podaje się pod symbolem | PN-EN 149+A1:2010 Rys. 12a; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (e) | Sprzęt ochrony układu oddechowego Półmaski filtrujące do ochrony przed cząstkami Wymaganie, badanie, znakowanie; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Patrz informacje dostarczone przez producenta | Wskazuje, że użytkownik powinien zapoznać się z instrukcja używania | PN-EN 149+A1:2010 Rys. 12b; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Sprzęt ochrony układu oddechowego Półmaski filtrujące do ochrony przed cząstkami Wymaganie, badanie, znakowanie; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
Zakres temperatur w warunkach przechowywania | Wskazuje zakres temperatur, na które ŚOI może być bezpiecznie narażony Znaki „xx” należy zastąpić górną i dolną granicą zakresu dopuszczalnej temperatury, odpowiednio | PN-EN 149+A1:2010 Rys. 12c; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Sprzęt ochrony układu oddechowego Półmaski filtrujące do ochrony przed cząstkami Wymaganie, badanie, znakowanie; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Maksymalna wilgotność względna w warunkach przechowywania | Wskazuje ŚOI, który wymaga ochrony przed wilgocią Znak „xx” należy zastąpić maksymalną wilgotnością | PN-EN 149+A1:2010 Rys. 12d; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Sprzęt ochrony układu oddechowego Półmaski filtrujące do ochrony przed cząstkami Wymaganie, badanie, znakowanie; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Ochrona przed chemikaliami | Wskazuje rękawice chroniące przed zagrożeniami chemicznymi; Znak „X” wskazuje typ rękawicy (A, B lub C); Znaki ”UVWXYZ” – wskazują badane substancje: - w przypadku rękawic typu A – pod piktogramem powinny być oznaczone literą wszystkie badane substancje chemiczne, - w przypadku rękawic typu B – tylko trzy badane substancje chemiczne powinny być oznaczone literą pod piktogramem; - w przypadku rękawic typu C - substancje nie są wypisywane; | EN ISO 374-1:2016, EN ISO 374-1:2016/A1:2018 (ISO 7000-2414) | Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 1: Terminologia i wymagania dotyczące skuteczności w zakresie ryzyka chemicznego |

|
Ochrona przed chemikaliami | Wskazuje rękawice chroniące przed zagrożeniami chemicznymi typu B Trzy badane substancje chemiczne powinny być oznaczone literą pod piktogramem | EN ISO 374-1:2016 (ISO 7000-2414) | Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 1: Terminologia i wymagania dotyczące skuteczności w zakresie ryzyka chemicznego |

|
Ochrona przed narażeniem na czynniki zakaźne | Wskazuje rękawice chroniące przed mikroorganizmami – wirusami, bakteriami i grzybami | EN ISO 374-5:2016 (ISO 7000-2491) | Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 5: Terminologia i wymagania dotyczące ryzyka przenikania mikroorganizmów |

|
Ochrona przed patogenami przenoszonymi przez krew | Wskazuje rękawice chroniące przed patogenami przenoszonymi przez krew | ISO 16604:2004 ASTM F1671 | Odzież chroniąca przed kontaktem z krwią i płynami ustrojowymi - Oznaczanie odporności materiałów na odzież ochronną na przenikanie patogenów krwiopochodnych - Metoda badania z użyciem bakteriofaga Phi-X 174 Standardowa metoda badania odporności materiałów stosowanych w odzieży ochronnej na przenikanie patogenów krwiopochodnych z wykorzystaniem bakteriofaga Phi-X174 jako systemu testowego |

|
Ochrona przed cytostatykami | Wskazuje rękawice chroniące przed cytostatykami | ASTM D6978 | Standardowa praktyka oceny odporności rękawic medycznych na przenikanie leków stosowanych w chemioterapii |

|
Dopuszczalny poziom jakości EN455-1, EN 374-2 | Wskazuje granicę akceptowanej jakości | EN 455-1:2020+A1:2022 EN ISO 374-2:2019 | Rękawice medyczne do jednorazowego użytku -- Część 1: Wymagania i badania na nieobecność dziur Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 2: Wyznaczanie odporności na przesiąkanie |
|
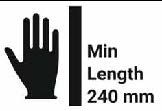
Minimalna długość rękawicy 240mm | Wskazuje, że minimalna długość rękawicy wynosi 240mm | ||

|
Dopuszczalny poziom jakości EN455-1, EN 374- 2 | Wskazuje granicę akceptowanej jakości | EN 455-1:2020+A1:2022 EN ISO 374-2:2019 | Rękawice medyczne do jednorazowego użytku -- Część 1: Wymagania i badania na nieobecność dziur Rękawice chroniące przed niebezpiecznymi substancjami chemicznymi i mikroorganizmami -- Część 2: Wyznaczanie odporności na przesiąkanie |

|
Ochrona przed patogenami | Wskazuje rękawice chroniące przed patogenami | ||
|
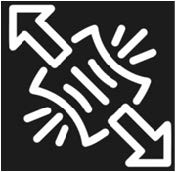
Rękawica rozciąga się we wszystkie strony | Wskazuje rękawice, które rozciągają się we wszystkie strony | ||

|
Możliwość stosowania przy ekranach dotykowych | Wskazuje rękawice, w których można obsługiwać ekrany dotykowe | ||

|
Kontakt z żywnością | Wskazuje rękawice odpowiednie do kontaktu z żywnością | Rozporządzenie (WE) nr 1935/2004 Parlamentu Europejskiego i Rady | Rozporządzenie (WE) nr 1935/2004 Parlamentu Europejskiego i Rady z dnia 27 października 2004 r. w sprawie materiałów i wyrobów przeznaczonych do kontaktu z żywnością |

|
Liczba rękawic | Wskazuje liczbę sztuk rękawic w opakowaniu | - | - |

|
Liczba par rękawic | Wskazuje liczbę par rękawic w opakowaniu | - | - |

|
Patrz informacje dostarczone przez producenta | Wskazuje rękawice specjalnego przeznaczenia (ochrona dłoni) – rękawice diagnostyczne i chirurgiczne; | EN-455-2:2024 (ISO 7000-1641) Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | EN 455-2:2024 - Rękawice medyczne jednorazowego użytku -- Część 2: Wymagania i badania dotyczące właściwości fizycznych; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Patrz informacje dla użytkownika | Wskazuje, że użytkownik powinien zapoznać się z informacjami dotyczącymi użytkowania | Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Nie prać | Wskazuje ŚOI, którego nie wolno prać | EN ISO 3758:2023 (ISO 7000-3123) Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
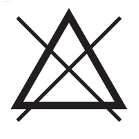
Nie używać wybielacza | Wskazuje ŚOI, do którego nie należy używać wybielacza | EN ISO 3758:2023 (ISO 7000-3124); Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Nie suszyć mechanicznie | Wskazuje ŚOI, którego nie powinno się suszyć w suszarce bębnowej | EN ISO 3758:2023 (ISO 7000-3109) Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Nie prasować | Wskazuje ŚOI, którego nie należy prasować | EN ISO 3758:2023 (ISO 7000-3113) Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
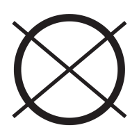
Nie czyścić chemicznie | Wskazuje ŚOI, którego nie należy czyścić chemicznie | EN ISO 3758:2023 (ISO 7000-3114) Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Tekstylia -- System oznaczania sposobu konserwacji z zastosowaniem symboli; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Materiał łatwopalny | Wskazuje ŚOI, który został wykonany z materiału łatwopalnego | ||
|
Jednostka opakowania | Wskazuje liczbę sztuk w opakowaniu | ISO 7000 Nr ref. symbolu 2794 | Symbole graficzne stosowane na urządzeniach |

|
Limit układania w stos | Wskazuje, że opakowania transportowe nie mogą być układane w pionie poza określoną liczbę, ani ze względu na rodzaj opakowania transportowego, ani z powodu charakteru samych przedmiotów. Liczbę „n” należy zastąpić maksymalną liczbą dozwolonych opakowań Liczba „n” nie obejmuje dolnego opakowania w stosie | ISO 7000 Nr ref. symbolu 2403; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |

|
Tą stroną w górę | Wskazuje prawidłową pozycję pionową opakowania transportowego | ISO 7000 Nr ref. symbolu 0623; Rozporządzenie PE i Rady (UE) 2016/425 Załącznik II, pkt.1.4. (a) | Symbole graficzne stosowane na urządzeniach; Rozporządzenie PE i Rady (UE) 2016/425 z dnia 9 marca 2016 r. w sprawie środków ochrony indywidualnej |
|
Nie używać haków | Wskazuje, że haki nie mogą być używane do przenoszenia opakowania transportowego | ||

|
Nie używać ostrych narzędzi | Wskazuje, że ostre narzędzia nie mogą być używane do otwierania opakowania transportowego | ||

|
Nie deptać | Wskazuje, że nie można stawać na opakowaniu transportowym | ||

|
Nadający się do przetworzenia | Wskazanie, że oznaczone opakowanie transportowe jest częścią procesu odzysku lub recyklingu | ISO 7000 Nr ref. symbolu 1135 | Symbole graficzne stosowane na urządzeniach |

|
Polietylen małej gęstości | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 1 Nr symbolu 4 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Tektura falista | Załącznik nr 2 Nr symbolu 1 | Załącznik nr 2 Nr symbolu 1 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Tektura płaska | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 2 Nr symbolu 2 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Papier | Wskazuje materiał, z którego wykonane jest opakowanie | Załącznik nr 2 Nr symbolu 3 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |

|
Mieszane | Wskazuje, że opakowanie wykonane jest z różnych/mieszanych materiałów | Załącznik nr 2 Nr symbolu 1 | Rozporządzenie Ministra Środowiska z dnia 3 września 2014 r. w sprawie wzorów oznakowania opakowań |